Искусственный желудочек сердца – (англ. VAD - Ventricular Assist Device) – механическое устройство, частично или полностью заменяющее функцию сердца при сердечной недостаточности. Дословный перевод: Желудочковое вспомогательное устройство.
Следует отличать понятия Искусственное сердце (англ. Total Artificial Heart ) и Искусственный желудочек сердца, так как последний заменяет только работу правого или левого желудочков сердца, или же обоих. В этих случаях имеются ввиду Правый искусственный желудочек сердца (англ. RVAD - Right Ventricular Assist Device) или Левый искусственный желудочек сердца (англ. LVAD - Left Ventricular Assist Device). Существует также Двойной искусственный желудочек сердца (англ. BiVAD – Biventricular Assist Device). Использование того или иного типа желудочкового вспомогательного устройства зависит от резистентности сосудов легкого. Левожелудочковые устройства используются наиболее часто, однако в случае повышенной резистентности сосудов легких стоит вопрос об использовании правых искусственных желудочках сердца.
Применение этих устройств в лечении тяжелой сердечной недостаточности рассматривается в двух аспектах. Первый – это «мостик» к трансплантации сердца (bridge to transplantation), т.е. устройство используется временно, пока пациент ожидает донорское сердце. Второй – это «мостик» к выздоровлению (bridge to recovery), когда, благодаря использованию искусственного желудочка сердца , восстанавливается функция сердечной мышцы.
В каких же случаях применяются желудочковые вспомогательные устройства в кардиохирургии?
1. Кардиогенный шок, ассоциированный с острым инфарктом миокарда
2. Посткардиотомический кардиогенный шок
3. Хроническая сердечная недостаточность в стадии декомпенсации
4. Миокардиты
5. Желудочковая аритмия
Стоит отметить, что в группу этих устройств можно было бы отнести и использование внутриаортальной баллонной контрапульсации (Intra-Aortic Balloon Pump), а также ЭКМО - экстракорпоральную мембранную оксигенацию (ECMO - Extracorporeal membrane oxygenation). Это, своего рода, тоже механическая и искусственная функция поддержки работы желудочков сердца. Однако мы рассмотрим их в следующих статьях.
 Принцип работы искусственных желудочков сердца заключается в механической разгрузке левого или правого желудочка сердца. Канюля имплантируется в верхушку левого желудочка, далее кровь через насос левого желудочкового вспомогательного устройства идет в канюлю, имплантируемую в аорту. В случае использования правого искусственного желудочка, кровь из правого желудочка через насос поступает в легочную артерию.
Принцип работы искусственных желудочков сердца заключается в механической разгрузке левого или правого желудочка сердца. Канюля имплантируется в верхушку левого желудочка, далее кровь через насос левого желудочкового вспомогательного устройства идет в канюлю, имплантируемую в аорту. В случае использования правого искусственного желудочка, кровь из правого желудочка через насос поступает в легочную артерию.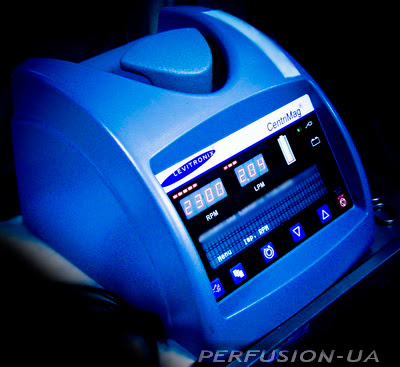
Levitronix CentriMag Blood Pumping System
CentriMag производства Levitronix – относится к устройствам нового поколения, обеспечивающих гемодинамическую поддержку с минимальной травмой клеточных элементов крови. Гемолиз оказывается минимальным. Устройство состоит из 3-х компонентов:
1. Одноразовый кровяной насос
2. Главная консоль управления и мотор
3. Дополнительная консоль управления и мотор

Устройство относится к временным. Т.е. может оказывать внешнюю гемодинамическую поддержку функции сердца (желудочков) до 30 дней. Максимальный объем перфузии до 9,9 литров в минуту на частоте 5500 оборотов в минуту. Объем первичного заполнения – прайм (priming volume) составляет всего 31 мл. Levitronix CentriMag прежде всего отличает компактность и транспортабельность, а также быстрая подготовка к использованию в экстренных случаях. Масса консоли составляет всего 6,6 кг.
Для применения в детской кардиохирургии разработан Levitronix PediVAS. Отличительная его особенность – объем прайма уменьшен до 14 мл.
В Европейских клиниках эти устройства уже активно используются, хотя в США они находятся в стадии апробации. Читайте подробнее здесь: De Robertis F, Birks EJ, Rogers P, et al: Clinical performance with the Levitronix Centrimag short-term ventricular assist device. J Heart Lung Transplant 2006; 25:181
Из устройств, работающих для временной поддержки функции желудочков сердца, можно назвать Cancion и Impella.
Из имплантируемых желудочковых вспомогательных устройств следует отметить те устройства, которые вошли в историю:
Вышеупомянутый Levitronix Centrimag был куплен компанией Thoratec в 2011 году. Теперь он называется Thoratec® CentriMag® Blood Pump.
Levacor VAD
Выпускался компанией World Heart. Тип устройства: пульсирующий. Был апробирован для использования в Северной Америке, Европейском Союзе и Японии.
Heartmate
Выпускался компанией: Thoratec. Тип устройства: пульсирующий. Был апробирован для использования в Северной Америке.
Heartmate II
Производитель: Thoratec. Апробирован для использования в Северной Америке и Европейском Союзе. В России Heartmate II впервые был имплантирован в клинике Бакулева (2007 год).
Incor и Excor
Производитель: Berlin Heart. Апробирован для использования в Европейском Союзе.
Наиболее интересная информация о технике имплантации искусственных желудочках сердца в интернете приведена ниже:
- Техника имплантации Искусственного желудочка Novacor Implantation technique of the Novacor left ventricular assist device Alain Pavie, Nils Reiss, and Stéphane Aubert
- Имплантация искусственного сердца (Cardiowest, Thoratec) Total artificial heart-implantation technique using the CardioWest or the Thoratec system Reiner Körfer, Aly El Banayosy, Michiel Morshuis, Gero Tenderich, Nils Reiss, and Latif Arusoglu
В схеме принципа работы LVAD использована иллюстрация Patrick J Lynch
Impella 2.5 черезкожный имплантируемый искусственный желудочек сердца.
AbioCor II - искусственное сердце Heart Mate II - искусственный желудочек сердца

 Наиболее интересные статьи о хирургическом лечении диссекции аорты можно прочитать здесь (полная версия на английском языке):
Наиболее интересные статьи о хирургическом лечении диссекции аорты можно прочитать здесь (полная версия на английском языке):